為全面貫徹中央關於加強智慧財產權保護的重要指示精神,深化落實「放管服」改革決策部署,積極回應經濟科技快速發展對審查規則的訴求,以及提高專利審查品質和審查效率,中國國家知識產權局 (CNIPA) 決定對《專利審查指南》作出修改,並已正式發佈,自2021年1月15日起施行。

圖片來源 : shutterstock、達志影像
CNIPA對《專利審查指南》作出的修改主要集中在第二部分第十章,共有7處,分別為第二部分第十章第3.5節、第二部分第十章第4.2.3節、第二部分第十章第5.1節、第二部分第十章第6.1節、第二部分第十章第9.2.1節、第二部分第十章第9.3.1.7節及第二部分第十章第9.4.2節。現分述如下。
(一)第二部分第十章第3.5節的修改
這部分主要是將《專利審查指南》第二部分第十章第3.5節細分為「3.5.1 審查原則」及 「3.5.2 藥品專利申請的補交實驗資料」,並於藥品專利申請的補交實驗資料的部分加入2個例子,將細節具體明確化。修改後條文如下:
3.5關於補交的實驗資料
3.5.1 審查原則
判斷說明書是否充分公開,以原說明書和權利要求書記載的內容為准。
對於申請日之後申請人為滿足專利法第二十二條第三款、第二十六條第三款等要求補交的實驗資料,審查員應當予以審查。補交實驗資料所證明的技術效果應當是所屬技術領域的技術人員能夠從專利申請公開的內容中得到的。
3.5.2 藥品專利申請的補交實驗資料
按照本章第3.5.1節的審查原則,給出涉及藥品專利申請的審查示例。
【例1】
權利要求請求保護化合物A,說明書記載了化合物A的製備實施例、降血壓作用及測定降血壓活性的實驗方法,但未記載實驗結果資料。為證明說明書充分公開,申請人補交了化合物A的降血壓效果資料。對於所屬技術領域的技術人員來說,根據原始申請文件的記載,化合物A的降血壓作用已經公開,補交實驗資料所要證明的技術效果能夠從專利申請文件公開的內容中得到。應該注意的是,該補交實驗資料在審查創造性時也應當予以審查。
【例2】
權利要求請求保護通式I化合物,說明書記載了通式I及其製備方法,通式I中多個具體化合物A、B等的製備實施例,也記載了通式I的抗腫瘤作用、測定抗腫瘤活性的實驗方法和實驗結果資料,實驗結果資料記載為實施例化合物對腫瘤細胞IC50值在10-100nM範圍內。為證明權利要求具備創造性,申請人補交了對比實驗資料,顯示化合物A的IC50值為15nM,而對比文化1化合物為87nM。對於所屬技術領域的技術人員來說,根據原始申請文件的記載,化合物A及其抗腫瘤作用已經公開,補交實驗資料所要證明的技術效果能夠從專利申請文件公開的內容中得到。應該注意的是,此時,審查員還需要結合補交實驗資料進一步分析權利要求請求保護的技術方案是否滿足創造性的要求。
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
第二部分第十章
3.5關於補交的實驗資料
判斷說明書是否充分公開,以原說明書和權利要求書記載的內容為准。
對於申請日之後補交的實驗資料,審查員應當予以審查。補交實驗資料所證明的技術效果應當是所屬技術領域的技術人員能夠從專利申請公開的內容中得到的。 |
第二部分第十章
3.5關於補交的實驗資料
3.5.1 審查原則
判斷說明書是否充分公開,以原說明書和權利要求書記載的內容為准。
對於申請日之後申請人為滿足專利法第二十二條第三款、第二十六條第三款等要求補交的實驗資料,審查員應當予以審查。補交實驗資料所證明的技術效果應當是所屬技術領域的技術人員能夠從專利申請公開的內容中得到的。
3.5.2 藥品專利申請的補交實驗資料
按照本章第3.5.1節的審查原則,給出涉及藥品專利申請的審查示例。
【例1】
權利要求請求保護化合物A,說明書記載了化合物A的製備實施例、降血壓作用及測定降血壓活性的實驗方法,但未記載實驗結果資料。為證明說明書充分公開,申請人補交了化合物A的降血壓效果資料。對於所屬技術領域的技術人員來說,根據原始申請文件的記載,化合物A的降血壓作用已經公開,補交實驗資料所要證明的技術效果能夠從專利申請文件公開的內容中得到。應該注意的是,該補交實驗資料在審查創造性時也應當予以審查。
【例2】
權利要求請求保護通式I化合物,說明書記載了通式I及其製備方法,通式I中多個具體化合物A、B等的製備實施例,也記載了通式I的抗腫瘤作用、測定抗腫瘤活性的實驗方法和實驗結果資料,實驗結果資料記載為實施例化合物對腫瘤細胞IC50值在10-100nM範圍內。為證明權利要求具備創造性,申請人補交了對比實驗資料,顯示化合物A的IC50值為15nM,而對比文件1化合物為87nM。對於所屬技術領域的技術人員來說,根據原始申請文件的記載,化合物A及其抗腫瘤作用已經公開,補交實驗資料所要證明的技術效果能夠從專利申請文件公開的內容中得到。應該注意的是,此時,審查員還需要結合補交實驗資料進一步分析權利要求請求保護的技術方案是否滿足創造性的要求。
|
(二)第二部分第十章第4.2.3節的修改
這部分只是些微的文辭修改,將《專利審查指南》第二部分第十章第4.2.3節最後一段中的「則應寫成性能限定型或者用途限定型」修改為「通常需要寫成性能限定型或者用途限定型」,將「在某些領域中,例如合金,通常應當寫明發明合金所固有的性質和/或用途。」修改為「在某些領域中,例如合金,通常應當寫明發明合金所固有的性能和/或用途。」
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
4.2.3組合物權利要求的其他限定
……
如果在說明書中僅公開了組合物的一種性能或者用途,則應寫成性能限定型或者用途限定型,例如(2)、(3)。在某些領域中,例如合金,通常應當寫明發明合金所固有的性質和/或用途。大多數藥品權利要求應當寫成用途限定型。
|
4.2.3組合物權利要求的其他限定
……
如果在說明書中僅公開了組合物的一種性能或者用途,則應通常需要寫成性能限定型或者用途限定型,例如(2)、(3)。在某些領域中,例如合金,通常應當寫明發明合金所固有的性質能和/或用途。大多數藥品權利要求應當寫成用途限定型。
|
(三)第二部分第十章第5.1節的修改
這部分是比較多的文辭修改,將《專利審查指南》第二部分第十章第5.1節中的第(1)項修改為:
(1)專利申請要求保護一種化合物的,如果在一份對比文件中記載了化合物的化學名稱、分子式(或結構式)等結構資訊,使所屬技術領域的技術人員認為要求保護的化合物已經被公開,則該化合物不具備新穎性,但申請人能提供證據證明在申請日之前無法獲得該化合物的除外。
如果依據一份對比文件中記載的結構資訊不足以認定要求保護的化合物與對比文件公開的化合物之間的結構異同,但在結合該對比文件記載的其他資訊,包括物理化學參數、製備方法和效果實驗資料等進行綜合考量後,所屬技術領域的技術人員有理由推定二者實質相同,則要求保護的化合物不具備新穎性,除非申請人能提供證據證明結構確有差異。
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
第二部分第十章
5.化學發明的新穎性
5.1 化合物的新穎性
(1) 專利申請要求保護一種化合物的,如果在一份對比文件裡已經提到該化合物,即推定該化合物不具備新穎性,但申請人能提供證據證明在申請日之前無法獲得該化合物的除外。這裡所謂「提到」的含義是:明確定義或者說明了該化合物的化學名稱、分子式(或結構式)、理化參數或製備方法(包括原料)。
例如,如果一份對比文件中所公開的化合物的名稱和分子式 (或結構式) 難以辨認或者不清楚,但該文件公開了與專利申請要求保護的化合物相同的理化參數或者鑒定化合物用的其他參數等,即推定該化合物不具備新穎性,但申請人能提供證據證明在申請日之前無法獲得該化合物的除外。
如果一份對比文件中所公開的化合物的名稱、分子式(或結構式)和理化參數不清楚,但該文件公開了與專利申請要求保護的化合物相同的製備方法,即推定該化合物不具備新穎性。 |
第二部分第十章
5.化學發明的新穎性
5.1 化合物的新穎性
(1) 專利申請要求保護一種化合物的,如果在一份對比文件裡中已經提到該化合物記載了化合物的化學名稱、分子式(或結構式)等結構資訊,使所屬技術領域的技術人員認為要求保護的化合物已經被公開,,即推定則該化合物不具備新穎性,但申請人能提供證據證明在申請日之前無法獲得該化合物的除外。這裡所謂「提到」的含義是:明確定義或者說明了該化合物的化學名稱、分子式(或結構式)、理化參數或製備方法(包括原料)。
如果依據一份對比文件中記載的結構資訊不足以認定要求保護的化合物與對比文件公開的化合物之間的結構異同,但在結合該對比文件記載的其他資訊,包括物理化學參數、製備方法和效果實驗數據等進行綜合考量後,所屬技術領域的技術人員有理由推定二者實質相同,則要求保護的化合物不具備新穎性,除非申請人能提供證據證明結構確有差異。
例如,如果一份對比文件中所公開的化合物的名稱和分子式(或結構式)難以辨認或者不清楚,但該文件公開了與專利申請要求保護的化合物相同的理化參數或者鑒定化合物用的其他參數等,即推定該化合物不具備新穎性,但申請人能提供證據證明在申請日之前無法獲得該化合物的除外。
如果一份對比文件中所公開的化合物的名稱、分子式(或結構式)和理化參數不清楚,但該文件公開了與專利申請要求保護的化合物相同的製備方法,即推定該化合物不具備新穎性。 |
(四)第二部分第十章第6.1節的修改
《專利審查指南》第二部分第十章第6.1節修改如下,並增加了2個例子 (例4、例5)。
6.1化合物的創造性
(1)判斷化合物發明的創造性,需要確定要求保護的化合物與最接近現有技術化合物之間的結構差異,並基於進行這種結構改造所獲得的用途和/或效果確定發明實際解決的技術問題,在此基礎上,判斷現有技術整體上是否給出了通過這種結構改造以解決所述技術問題的技術啟示。
需要注意的是,如果所屬技術領域的技術人員在現有技術的基礎上僅僅通過合乎邏輯的分析、推理或者有限的試驗就可以進行這種結構改造以解決所述技術問題,得到要求保護的化合物,則認為現有技術存在技術啟示。
(2)發明對最接近現有技術化合物進行的結構改造所帶來的用途和/或效果可以是獲得與已知化合物不同的用途,也可以是對已知化合物某方面效果的改進。在判斷化合物創造性時,如果這種用途的改變和/或效果的改進是預料不到的,則反映了要求保護的化合物是非顯而易見的,應當認可其創造性。
(3)需要說明的是,判斷化合物發明的創造性時,如果要求保護的技術方案的效果是已知的必然趨勢所導致的,則該技術方案沒有創造性。例如,現有技術的一種殺蟲劑A-R,其中R為C1-3的烷基,並且已經指出殺蟲效果隨著烷基C原子數的增加而提高。如果某一申請的殺蟲劑是A-C4H9,殺蟲效果比現有技術的殺蟲效果有明顯提高。由於現有技術中指出了提高殺蟲效果的必然趨勢,因此該申請不具備創造性。
(4)創造性判斷示例
【例1】
現有技術:
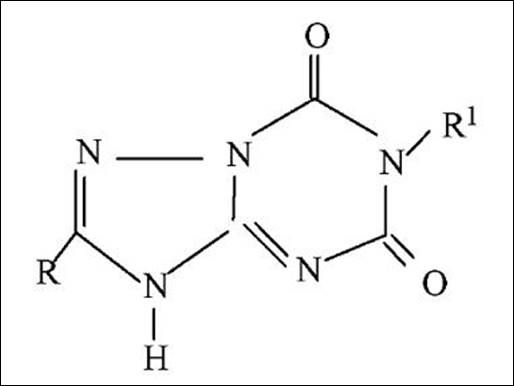
(Ia)
申請:
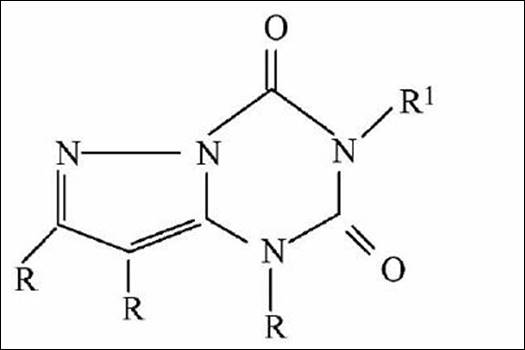
(Ib)
(Ⅰb)與(Ⅰa)的母核結構不同,但二者具有相同的用途。所屬技術領域的技術人員通常認為結構接近的化合物具有相同或類似的用途,且結構接近通常是指化合物具有相同的基本核心部分或者基本的環。現有技術中不存在對(Ⅰa)的基本的環進行改造以獲得(Ⅰb)且用途不變的技術啟示,故(Ⅰb)具有創造性。
【例2】
現有技術:H2N-C6H4-SO2NHR1 (Ⅱa)
申請:H2N-C6H4-SO2-NHCONHR1 (Ⅱb)
(Ⅱb)是在(Ⅱa)NHR1結構片段中插入了-CONH-,二者用途完全不同,(Ⅱa)磺胺是抗菌素,(Ⅱb)磺醯脲是抗糖尿藥。所屬技術領域的技術人員沒有動機將抗菌素中的R1改造為CONHR1以獲得抗糖尿藥,故(Ⅱb)具有創造性。
【例3】
現有技術:H2N-C6H4-SO2NHCONHR1(Ⅲa)
申請:H3C-C6H4-SO2NHCONHR1(Ⅲb)
(Ⅲa)氨基-磺醯脲與(Ⅲb)甲基-磺醯脲之間僅存在NH2與CH3的結構差異,兩者均為抗糖尿藥,且效果相當,(Ⅲb)相對於(Ⅲa)為所屬技術領域提供了另一種抗糖尿藥。由於NH2與CH3是經典一價電子等排體,所屬技術領域的技術人員為獲得相同或相當的抗糖尿活性有動機進行這種電子等排體置換,故(Ⅲb)無創造性。
【例4】
現有技術:
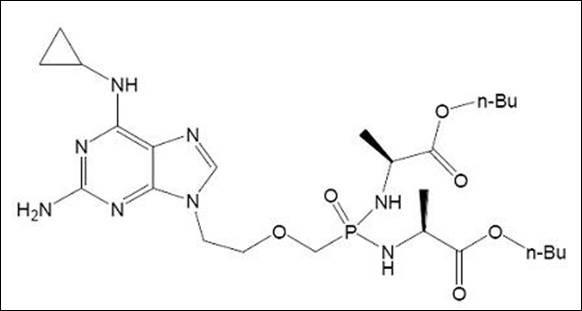
(Ⅳa)
申請:
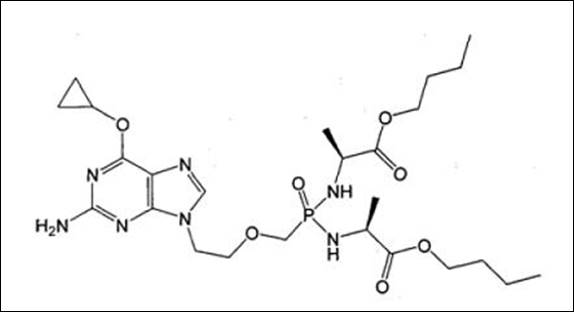
(Ⅳb)
(Ⅳb)與(Ⅳa)化合物的區別僅在於嘌呤6-位上以-O-替換了-NH-。儘管-O-與-NH-為所屬技術領域公知的經典電子等排體,但(Ⅳb)的癌細胞生長抑制活性比(Ⅳa)提高約40倍,(Ⅳb)相對於(Ⅳa)取得了預料不到的技術效果,由此反映(Ⅳb)是非顯而易見的,故(Ⅳb)具有創造性。
【例5】
現有技術:
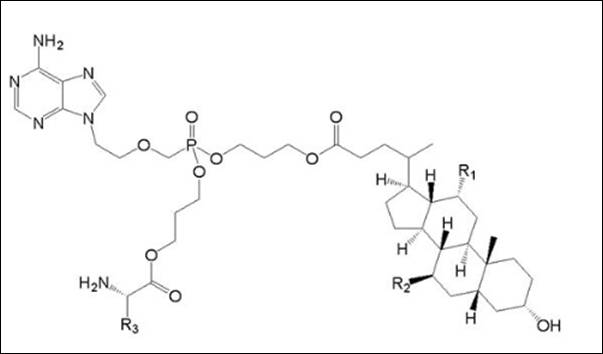
(Ⅴa)
其中R1=OH, R2=H且R3=CH2CH(CH3)2。
申請:
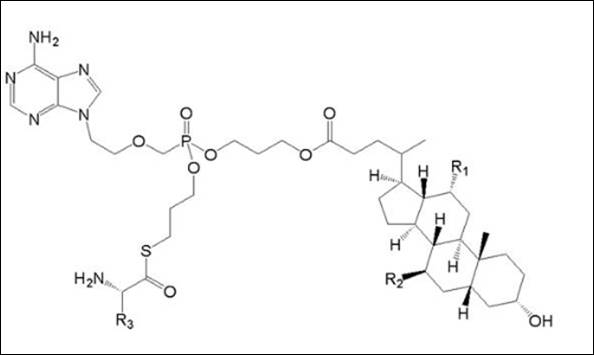
(Ⅴb)
其中R1和R2選自H或OH,R3選自C1-6烷基,並包括了R1=OH, R2=H且R3=CHCH3CH2CH3的具體化合物(Ⅴb1)。且(Ⅴb1)的抗乙肝病毒活性明顯優於(Ⅴa)。
當要求保護(Ⅴb)通式化合物時,(Ⅴb)與(Ⅴa)的區別僅在於磷醯基烷基與氨基酸殘基之間的連接原子不同,(Ⅴb)為-S-,而(Ⅴa)為-O-。(Ⅴb)通式化合物相對於(Ⅴa)為所屬技術領域提供了另一種抗乙肝病毒藥。由於-S-與-O-性質接近,為獲得同樣具有抗乙肝病毒活性的其他藥物,所屬技術領域的技術人員有動機進行這種替換並獲得所述(Ⅴb)通式化合物,故(Ⅴb)無創造性。
當要求保護(Ⅴb1)具體化合物時,(Ⅴb1)與(Ⅴa)的區別不僅在於上述連接原子不同,而且R3位取代基亦不相同,(Ⅴb1)的抗乙肝病毒活性明顯優於(Ⅴa)。現有技術中不存在通過所述結構改造以提升抗乙肝病毒活性的技術啟示,故(Ⅴb1)具有創造性。
(五) 第二部分第十章第9.2.1節的修改
這部分將《專利審查指南》第二部分第十章第9.2.1節第(4)項中的「其中包括位於我國北京的中國微生物菌種保藏管理委員會普通微生物中心(CGMCC)和位於武漢的中國典型培養物保藏中心(CCTCC)。」修改為「其中包括位於我國北京的中國微生物菌種保藏管理委員會普通微生物中心(CGMCC)、位於武漢的中國典型培養物保藏中心(CCTCC)和位於廣州的廣東省微生物菌種保藏中心(GDMCC)。」
|
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
第二部分第十章
9.2 說明書的充分公開
9.2.1 生物材料的保藏
(4)國家知識產權局認可的保藏單位是指布達佩斯條約承認的生物材料樣品國際保藏單位,其中包括位於我國北京的中國微生物菌種保藏管理委員會普通微生物中心(CGMCC)和位於武漢的中國典型培養物保藏中心(CCTCC)。 |
第二部分第十章
9.2 說明書的充分公開
9.2.1 生物材料的保藏
(4)國家知識產權局認可的保藏單位是指布達佩斯條約承認的生物材料樣品國際保藏單位,其中包括位於我國北京的中國微生物菌種保藏管理委員會普通微生物中心(CGMCC)和、位於武漢的中國典型培養物保藏中心(CCTCC)和位於廣州的廣東省微生物菌種保藏中心(GDMCC)。 |
(六)第二部分第十章第9.3.1.7節的修改
《專利審查指南》第二部分第十章第9.3.1.7節修改如下:
9.3.1.7單克隆抗體
針對單克隆抗體的權利要求可以用結構特徵限定,也可以用產生它的雜交瘤來限定。
【例如】
(1)抗原A的單克隆抗體,其包含氨基酸序列如SEQ ID NO:1-3所示的VHCDR1、VHCDR2和VHCDR3,和氨基酸序列如SEQ ID NO:4-6所示的VLCDR1、VLCDR2和VLCDR3。
(2)抗原A的單克隆抗體,由保藏號為CGMCC NO:xxx的雜交瘤產生。
|
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
第二部分第十章
9.3生物技術領域發明的權利要求
9.3.1涉及遺傳工程的發明
9.3.1.7單克隆抗體
針對單克隆抗體的權利要求可以用產生它的雜交瘤來限定。
【例如】
抗原A的單克隆抗體,由保藏號為CGMCC NO:xxx的雜交瘤產生。
|
第二部分第十章
9.3生物技術領域發明的權利要求
9.3.1涉及遺傳工程的發明
9.3.1.7單克隆抗體
針對單克隆抗體的權利要求可以用結構特徵限定,也可以用產生它的雜交瘤來限定。
【例如】
抗原A的單克隆抗體,由保藏號為CGMCC NO:xxx的雜交瘤產生。
(1)抗原A的單克隆抗體,其包含氨基酸序列如SEQ ID NO:1-3所示的VHCDR1、VHCDR2和VHCDR3,和氨基酸序列
如SEQ ID NO:4-6所示的VLCDR1、VLCDR2和VLCDR3。
(2)抗原A的單克隆抗體,由保藏號為CGMCC NO:xxx的雜交瘤產生。 |
(七)第二部分第十章第9.4.2節的修改
這一部分修改比較多,共有7大部分。
(1)在《專利審查指南》第二部分第十章第9.4.2節創造性標題下新增三段,內容如下:
生物技術領域發明創造性的判斷,同樣要判斷發明是否具備突出的實質性特點和顯著的進步。判斷過程中,需要根據不同保護主題的具體限定內容,確定發明與最接近的現有技術的區別特徵,然後基於該區別特徵在發明中所能達到的技術效果確定發明實際解決的技術問題,再判斷現有技術整體上是否給出了技術啟示,基於此得出發明相對於現有技術是否顯而易見。
生物技術領域的發明創造涉及生物大分子、細胞、微生物個體等不同水準的保護主題。在表徵這些保護主題的方式中,除結構與組成等常見方式以外,還包括生物材料保藏號等特殊方式。創造性判斷需要考慮發明與現有技術的結構差異、親緣關係遠近和技術效果的可預期性等。
以下,示出本領域不同保護主題創造性判斷中的一些具體情形。
(2)將《專利審查指南》第二部分第十章第9.4.2.1節第(1)項修改如下:
1. 基因
如果某結構基因編碼的蛋白質與已知的蛋白質相比,具有不同的氨基酸序列,並具有不同類型的或改善的性能,而且現有技術沒有給出該序列差異帶來上述性能變化的技術啟示,則編碼該蛋白質的基因發明具有創造性。
如果某蛋白質的氨基酸序列是已知的,則編碼該蛋白質的基因的發明不具有創造性。如果某蛋白質已知而其氨基酸序列是未知的,那麼只要本領域技術人員在該申請提交時可以容易地確定其氨基酸序列,編碼該蛋白質的基因發明就不具有創造性。但是,上述兩種情形下,如果該基因具有特定的碱基序列,而且與其他編碼所述蛋白質的、具有不同碱基序列的基因相比,具有本領域技術人員預料不到的效果,則該基因的發明具有創造性。
如果一項發明要求保護的結構基因是一個已知結構基因的可自然獲得的突變的結構基因,且該要求保護的結構基因與該已知結構基因源於同一物種,也具有相同的性質和功能,則該發明不具備創造性。
(3) 在《專利審查指南》第二部分第十章第9.4.2.1節中增加第(2)項多肽或蛋白質,內容如下:
2. 多肽或蛋白質
如果發明要求保護的多肽或蛋白質與已知的多肽或蛋白質在氨基酸序列上存在區別,並具有不同類型的或改善的性能,而且現有技術沒有給出該序列差異帶來上述性能變化的技術啟示,則該多肽或蛋白質的發明具有創造性。
(4) 將《專利審查指南》第二部分第十章第9.4.2.1節中的「(2)重組載體」修改為「(3)重組載體」,並在原有內容前插入一段,內容如下:
如果發明針對已知載體和/或插入基因的結構改造實現了重組載體性能的改善,而且現有技術沒有給出利用上述結構改造以改善性能的技術啟示,則該重組載體的發明具有創造性。
(5) 將《專利審查指南》第二部分第十章第9.4.2.1節中的「(3)轉化體」修改為「(4)轉化體」,並在原有內容前插入一段,內容如下:
如果發明針對已知宿主和/或插入基因的結構改造實現了轉化體性能的改善,而且現有技術沒有給出利用上述結構改造以改善性能的技術啟示,則該轉化體的發明具有創造性。
(6) 將《專利審查指南》第二部分第十章第9.4.2.1節中的「(4)融合細胞」修改為「(5)融合細胞」。
(7) 將《專利審查指南》第二部分第十章第9.4.2.1節中的「(5)單克隆抗體」修改為「(6)單克隆抗體」,並將內容整體修改為:
如果抗原是已知的,採用結構特徵表徵的該抗原的單克隆抗體與已知單克隆抗體在決定功能和用途的關鍵序列上明顯不同,且現有技術沒有給出獲得上述序列的單克隆抗體的技術啟示,且該單克隆抗體能夠產生有益的技術效果,則該單克隆抗體的發明具有創造性。
如果抗原是已知的,並且很清楚該抗原具有免疫原性(例如由該抗原的多克隆抗體是已知的或者該抗原是大分子多肽就能得知該抗原明顯具有免疫原性),那麼僅用該抗原限定的單克隆抗體的發明不具有創造性。但是,如果該發明進一步由分泌該抗原的單克隆抗體的雜交瘤限定,並因此使其產生了預料不到的效果,則該單克隆抗體的發明具有創造性。
《專利審查指南》 (2010年2月1日起施行) |
《專利審查指南》(根據公告第三九一號修正)(2021年1月15日起施行) |
第二部分第十章
9.4.2創造性
9.4.2.1涉及遺傳工程的發明
(1)基因
如果在申請的發明中,某蛋白質已知而其氨基酸序列是未知的,那麼只要本領域技術人員在該申請提交時可以容易地確定其氨基酸序列,編碼該蛋白質的基因發明就不具有創造性。但是,如果該基因具有特定的碱基序列,而且與其他編碼所述蛋白質的、具有不同碱基序列的基因相比,具有本領域技術人員預料不到的效果,則該基因的發明具有創造性。
如果某蛋白質的氨基酸序列是已知的,則編碼該蛋白質的基因的發明不具有創造性。但是,如果該基因具有特定的堿基序列,而且與其他編碼所述蛋白質的、具有不同堿基序列的基因相比,具有本領域技術人員預料不到的效果,則該基因的發明具有創造性。
如果一項發明要求保護的結構基因是一個已知結構基因的可自然獲得的突變的結構基因,且該要求保護的結構基因與該已知結構
基因源於同一物種,也具有相同的性質和功能,則該發明不具備創造性。
(2)重組載體
如果載體與插入的基因都是已知的,通常由它們的結合所得到的重組載體的發明不具有創造性。但是,如果由它們的特定結合形成的重組載體的發明與現有技術相比具有預料不到的技術效果,則該重組載體的發明具有創造性。
(3)轉化體
如果宿主與插入的基因都是已知的,通常由它們的結合所得到的轉化體的發明不具有創造性。但是,如果由它們的特定結合形成的轉化體的發明與現有技術相比具有預料不到的技術效果,則該轉化體的發明具有創造性。
(4)融合細胞
如果親代細胞是已知的,通常由這些親代細胞融合所得到的融合細胞的發明不具有創造性。但是,如果該融合細胞與現有技術相比具有預料不到的技術效果,則該融合細胞的發明具有創造性。
(5)單克隆抗體
如果抗原是已知的,並且很清楚該抗原具有免疫原性(例如由該抗原的多克隆抗體是已知的或者該抗原是大分子多肽就能得知該抗原明顯具有免疫原性),那麼該抗原的單克隆抗體的發明不具有創造性。但是,如果該發明進一步由其他特徵等限定,並因此使其產生了預料不到的效果,則該單克隆抗體的發明具有創造性。
|
第二部分第十章
9.4.2創造性
生物技術領域發明創造性的判斷,同樣要判斷發明是否具備突出的實質性特點和顯著的進步。判斷過程中,需要根據不同保護主題的具體限定內容,確定發明與最接近的現有技術的區別特徵,然後基於該區別特徵在發明中所能達到的技術效果確定發明實際解決的技術問題,再判斷現有技術整體上是否給出了技術啟示,基於此得出發明相對於現有技術是否顯而易見。
生物技術領域的發明創造涉及生物大分子、細胞、微生物個體等不同水準的保護主題。在表徵這些保護主題的方式中,除結構與組成等常見方式以外,還包括生物材料保藏號等特殊方式。創造性判斷需要考慮發明與現有技術的結構差異、親緣關係遠近和技術效果的可預期性等。
以下,示出本領域不同保護主題創造性判斷中的一些具體情形。
9.4.2.1涉及遺傳工程的發明
(1)基因
如果在申請的發明中,某結構基因編碼的蛋白質與已知的蛋白質相比,具有不同的氨基酸序列,並具有不同類型的或改善的性能,而且現有技術沒有給出該序列差異帶來上述性能變化的技術啟示,則編碼該蛋白質的基因發明具有創造性。
如果某蛋白質的氨基酸序列是已知的,則編碼該蛋白質的基因的發明不具有創造性。如果某蛋白質已知而其氨基酸序列是未知的,那麼只要本領域技術人員在該申請提交時可以容易地確定其氨基酸序列,編碼該蛋白質的基因發明就不具有創造性。但是,上述兩種情形下,如果該基因具有特定的碱基序列,而且與其他編碼所述蛋白質的、具有不同碱基序列的基因相比,具有本領域技術人員預料不到的效果,則該基因的發明具有創造性。
如果某蛋白質的氨基酸序列是已知的,則編碼該蛋白質的基因的發明不具有創造性。但是,如果該基因具有特定的堿基序列,而且與其他編碼所述蛋白質的、具有不同碱基序列的基因相比,具有本領域技術人員預料不到的效果,則該基因的發明具有創造性。
如果一項發明要求保護的結構基因是一個已知結構基因的可自然獲得的突變的結構基因,且該要求保護的結構基因與該已知結構基因源於同一物種,也具有相同的性質和功能,則該發明不具備創造性。
(2)多肽或蛋白質
如果發明要求保護的多肽或蛋白質與已知的多肽或蛋白質在氨基酸序列上存在區別,並具有不同類型的或改善的性能,而且現有技術沒有給出該序列差異帶來上述性能變化的技術啟示,則該多肽或蛋白質的發明具有創造性。
(23)重組載體
如果發明針對已知載體和/或插入基因的結構改造實現了重組載體性能的改善,而且現有技術沒有給出利用上述結構改造以改善性能的技術啟示,則該重組載體的發明具有創造性。
如果載體與插入的基因都是已知的,通常由它們的結合所得到的重組載體的發明不具有創造性。但是,如果由它們的特定結合形成的重組載體的發明與現有技術相比具有預料不到的技術效果,則該重組載體的發明具有創造性。
(34)轉化體
如果發明針對已知宿主和/或插入基因的結構改造實現了轉化體性能的改善,而且現有技術沒有給出利用上述結構改造以改善性能的技術啟示,則該轉化體的發明具有創造性。
如果宿主與插入的基因都是已知的,通常由它們的結合所得到的轉化體的發明不具有創造性。但是,如果由它們的特定結合形成的轉化體的發明與現有技術相比具有預料不到的技術效果,則該轉化體的發明具有創造性。
(45)融合細胞
如果親代細胞是已知的,通常由這些親代細胞融合所得到的融合細胞的發明不具有創造性。但是,如果該融合細胞與現有技術相比具有預料不到的技術效果,則該融合細胞的發明具有創造性。
(56)單克隆抗體
如果抗原是已知的,採用結構特徵表徵的該抗原的單克隆抗體與已知單克隆抗體在決定功能和用途的關鍵序列上明顯不同,且現有技術沒有給出獲得上述序列的單克隆抗體的技術啟示,且該單克隆抗體能夠產生有益的技術效果,則該單克隆抗體的發明具有創造性。
如果抗原是已知的,並且很清楚該抗原具有免疫原性(例如由該抗原的多克隆抗體是已知的或者該抗原是大分子多肽就能得知該抗原明顯具有免疫原性),那麼僅用該抗原限定的單克隆抗體的發明不具有創造性。但是,如果該發明進一步由其他特徵等分泌該抗原的單克隆抗體的雜交瘤限定,並因此使其產生了預料不到的效果,則該單克隆抗體的發明具有創造性。 |
參考資料:
- 国家知识产权局关于修改《专利审查指南》的公告(第391号)
- 《专利审查指南》修改对照表
| 作者: |
李淑蓮 |
| 現任: |
北美智權報主編 |
| 學歷: |
文化大學新聞研究所 |
| 經歷: |
半導體科技雜誌(SST-Taiwan)總編輯
CompuTrade International總編輯
日本電波新聞 (Dempa Shinbun) 駐海外記者
日經亞洲電子雜誌 (台灣版) 編輯 |
|
|
|
| Facebook |
|
在北美智權報粉絲團上追踪我們 |
     |
|
|
|
|
|
|
|

