中国的药品专利纠纷早期解决机制,指的是衔接药品上市审批程序与药品专利纠纷解决程序的制度。2020年10月,在新修正的《专利法》)第76条中,引入药品专利纠纷早期解决的相关规定,明确由国务院药品监督管理部门和国务院专利行政部门制定药品上市许可审批,与药品上市许可申请阶段专利纠纷解决的具体办法。
而在2021年7月4日,国家药品监督管理局和国家知识产权局联合发布了《药品专利纠纷早期解决机制实施办法(试行)》,对于首个挑战专利成功并首个获批上市的化学仿制药,给予12个月市场独占期,并自发布之日开始施行。
图片来源:Pixabay
药品专利纠纷早期解决的途径
根据《药品专利纠纷早期解决机制实施办法(试行)》规定,专利权人或者利害关系人若对四类专利声明有异议,可以就申请上市药品的相关技术方案是否落入相关专利权保护范围,向人民法院提起诉讼,或是向国务院专利行政部门请求行政裁决。在规定的期限内,专利权人可以自行选择司法途径或行政途径。如果当事人选择向国务院专利行政部门请求行政裁决,对行政裁决不服又向人民法院提起行政诉讼的,并不会延长等待期。若专利权人或者利害关系人未在规定期限内提起诉讼或请求行政裁决,仿制药申请人可以按相关规定提起诉讼或者请求行政裁决,以确认其相关药品技术方案不落入相关专利权保护范围。
图一、药品专利连结中的四类声明

图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
中国药品专利连结的相关规定在《专利法》第76条。药品上市审评审批过程中,药品上市许可申请人与有关专利权人或者利害关系人,因申请注册的药品相关的专利权产生纠纷的,相关当事人可以向人民法院起诉,请求就申请注册的药品相关技术方案是否落入他人药品专利权保护范围作出判决。国务院药品监督管理部门在规定的期限内,可以根据人民法院生效裁判,作出是否暂停批准相关药品上市的决定。药品上市许可申请人与有关专利权人或者利害关系人也可以就申请注册的药品相关的专利权纠纷,向国务院专利行政部门请求行政裁决。
图二、中国药品专利连结制度运行机制
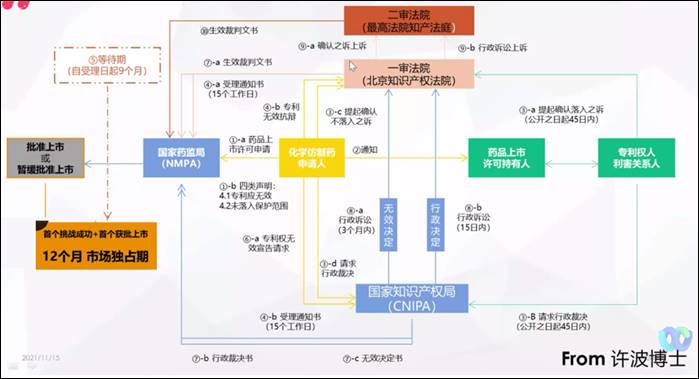
图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
知元同创知识产权代理事务所执行合伙人刘元霞解释,对权利人而言,《专利法》第76条的好处在于可以选择双途径救济,且以法院优先,即便已求助行政途径,也可以在法院立案。在实施办法落地后,也确认了只有权利人可以先启动程序,仿制药企业在发起声明后需要等待45天,而原研药企业则一定会将45天的权利用尽。
仿制药专利申请人挑战首仿药
根据试行办法第11条,对首个挑战专利成功并首个获批上市的化学仿制药,将给予市场独占期。国务院药品监督管理部门在该药品获批之日起12个月内,不再批准同品种仿制药上市(共同挑战专利成功的除外);市场独占期以不超过被挑战药品的原专利期为限。市场独占期内,国家药品审评机构不停止技术审查。刘元霞表示,挑战专利成功是指化学仿制药申请人提交四类声明,且根据其提出的宣告专利权无效请求,相关专利权被宣告无效,因而仿制药可获批上市。这里涉及对四类声明的理解:4.1类认为落入但无效,4.2类认为不落入,无论是做了4.1类声明或是4.2类声明,都可以发起专利无效的挑战。因此,仿制药申请人若能提交四类声明,且发起专利无效挑战,一但专利被宣告无效,就可能获得首家挑战成功的机会。
刘元霞认为,登记平台中相关专利有产品、组合物和用途等类型,但一般的仿制药仅落入其中一项或两项专利,可以仅针对有落入风险的专利发起挑战,避免提起过多诉讼程序,有利于仿制药申请人及早解决纠纷。
中国专利连结相关专利类型,分为化合物、组合物和用途;非专利连结相关专利类型则有晶型、制备方法和检测方法。刘元霞统计近五年来的中国药品专利的无效案件,涵盖化合物、制剂、用途、晶型四种类型,同一个专利只限统计一次,而且以最终的决定为准;部分无效的专利只要核心产品能够保留,就归为未无效之列。虽然数据可能有遗漏,但可参考整体趋势。从全部无效案件量观察,「用途」是最难被无效的,其次是化合物、制剂,最后是晶型。其中,制剂整体无效的成功率为60%,但分析2021年的案件会发现,只有「制剂」的无效成功率是不减反升的。
图三、中国药品专利无效成功率
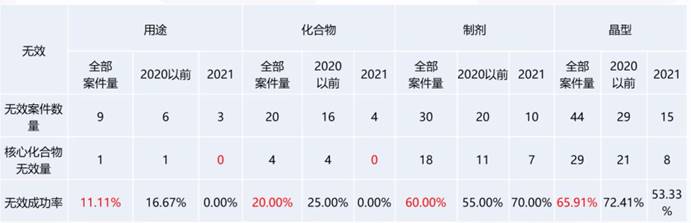
图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
药品专利保护期补偿制度
专利期延长制度(patent term extension,简称PTE),指的是药品专利保护期补偿,申请主体为专利权人,条件是中国获批上市的新药发明专利。根据中国《专利法》42条规定,专利补偿期限一般不超过五年,新药上市后总有效专利权期限不超过十四年。
图四、中国专利补偿期限
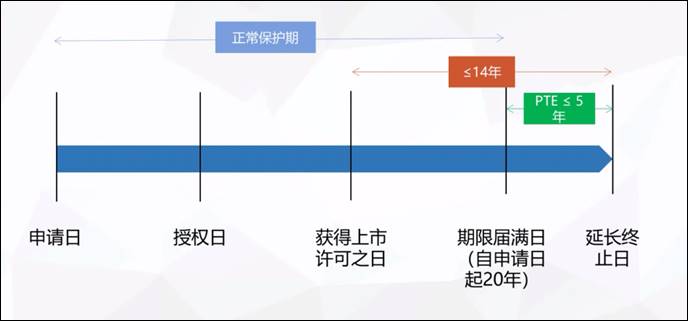
图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
中国国务院药品监督管理部门负责批准上市的创新药和符合规定的改良型新药,对于药物活性物质的产品专利、制备方法专利或者医药用途专利,可以给予药品专利期限补偿。而请求药品专利期限补偿,应满足以下条件:
(1)求补偿的专利授权公告日应当早于药品上市许可申请获得批准之日;
(2)提出补偿请求时,该专利权处于有效状态;
(3)该专利尚未获得过药品专利期限补偿;
(4)获得上市许可的新药相关技术方案应当落入请求补偿的专利权利要求的保护范围;
(5)一个药品同时存在多项专利的,只能请求对其中一项专利给予药品专利期限补偿;
(6)一项专利同时涉及多个药品的,只能对一个药品就该专利提出药品专利期限补偿请求。
刘元霞指出,大部分专利权利人比较关心的是专利期限的问题,若是一个药品同时存在多项专利,一般会选择保护期最长的。
PTE延长的审批流程
根据审查指南(征求意见稿)规定,专利权人请求药品专利补偿,应当自药品上市许可申请获得批准之日起,三个月内向专利局提出请求,并缴纳相应费用。专利局可对符合条件的药品专利给予药品期限补偿,以弥补在专利有效期内,该新药上市审批所占用的时间。药品专利补偿期限的计算方式为:药品上市许可申请获得批准之日减去专利申请日,再减去五年所得的时间。刘元霞指出,该补偿期限不超过五年,且该药品上市许可申请批准后总有效专利权期限不超过14年。这种计算方式可谓是有些简单粗暴,计算得到的补偿期限与企业实际想要获得的期限相比更短。此外,中国对PTE延长的审批流程规定得不明确,或许未来能参考美国PTE相关程序,对延长期的审批流程做出更细致的规定。
如何进行专利声明
化学仿制药申请人、中药同名同方药申请人、生物类似药申请人提交药品上市许可申请时,应当对照已在中国上市药品专利信息登记平台公开的专利信息,针对被仿制药每一件相关的药品专利作出声明。仿制药申请被受理后10个工作日内,仿制药申请人应当将相应声明及声明依据通知上市许可持有人。其中,声明未落入相关专利权保护范围的,声明依据应包括仿制药技术方案,与相关专利的权利要求对比表,以及相关技术等数据。
图五、中国上市药品专利登记信息平台示意图
图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
截止至2021年11月14日,共有919条专利信息登记信息,其中有612条做出专利声明。而做出专利声明中,共有12个四类声明,其中只有5个品种、共6项专利,做出了4.1类声明。
图六、中国上市药品专利信息登记平台——专利信息公示和专利声明
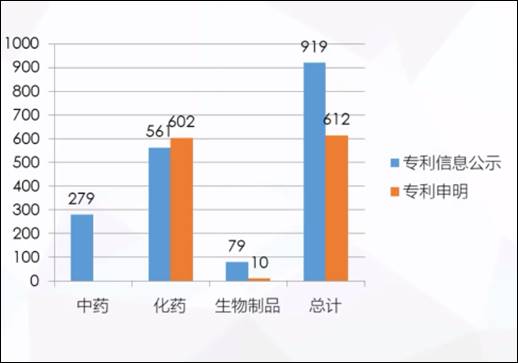
图片来源:2021/11/15,「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
首仿药专利挑战策略
刘元霞提醒,若想成为首仿药,可以关注中国专利信息登记平台上的登记信息,因为权利人或利害关系人会就相关产品的状态,在登记平台上及时更正。一旦申报信息公开,为尽可能争取到首仿,无效请求也会在第一时间提出。所以,同品种的其他企业关注到该信息后,能够大致判断公司在该品种上的竞争力,以及是否有首仿机会。值得注意的是,首家申报的企业并非就会首家获批,因此,第二至第五家申报的企业仍然有机会获得首家获批的资格。
另外,专利权利人请求药品专利期限补偿,应从药品上市许可获得批准之日起三个月内向专利局提出请求,因此关注PTE相关讯息,对仿制药企业的影响是非常大的。
数据源:
- 2021/11/15,专利师公会主办「中国药品专利纠纷早期解决机制下首仿药专利挑战策略」,刘元霞简报
- 2021/7/4,中国国家药监局、国家知识产权局关于发布《药品专利纠纷早期解决机制实施办法(试行)》的公告(2021年第89号)
好消息~北美智权报有微信公众号了!
《北美智权报》内容涵盖世界各国的知识产权新闻、重要的侵权诉讼案例分析、法规解析,以及产业与技术新知等等。
立即关注北美智权微信公众号→ NAIP_IPServices
~欢迎读者分享与转发~ |
 |
|
| 作者: |
吴碧娥 |
| 现任: |
北美智权报资深编辑 |
| 学历: |
(台湾)政治大学新闻研究所 |
| 经历: |
骅讯电子总经理室特助
经济日报财经组记者
东森购物总经理室经营企划 |
|
|
|

