Eli Lilly公司推出的Alimta(爱宁达注射剂)是临床常用的抗癌药物。在Alimta的药物结构专利到期后Eli Lilly公司凭借其后续申请的「抗叶酸组合的治疗方法专利」(’209号专利)成功抵御无数欲藉由「老药新用」策略进军此块丰厚市场的学名药厂。本文藉2019年9月和2020年12月等两则CAFC判决,说明原开发药厂如何主张均等论将均等范围扩张至系争药物的所有剂型和申请历史禁反言的攻防。

图片来源:iStockphoto
「老药新用」之新药开发策略,具开发时程较短、开发成本较低及投资成功率较高等优点。制药厂商不需投入大笔研发经费与时间成本创造全新畅销药物,而是将已上市的药物透过新剂型、新复方(组合型药品)、新适应症及新给药途径延续或甚至开拓全新的商业价值。在美国,FDA (U.S. Food and Drug Administration, 食品药物管理署) 将「老药新用」策略下的药物研发及上市申请途径规范在505(b)(2)。
从专利与产业交会的角度观之,相较从零开始研发全新药物,「老药新用」犹如搭载新兴或中小型制药厂商开往市场的直达车,但开发他人老药来新用的药厂仍必须防范原开发药厂早已在该直达的道路埋藏着阻挡去路的专利地雷。相对而言,原开发药厂亦可持续研究自家药物潜在的新剂型、新复方(组合型药品)、新适应症及新给药途径,积极申请专利和布局,以形成阻挡学名药厂进入市场的阻碍,延长自家畅销药物的生命周期,巩固独占市场下的丰厚利润。
案件背景
Alimta®(爱宁达注射剂)是临床常用的抗癌药物。自2002年上市后,Eli Lilly公司积极拓展的适应症版图持续开枝散叶,使其成为该公司最畅销的产品之一。Alimta®的活性药物成份为「培美曲塞」(pemetrexed),该化合物是一种叶酸拮抗剂,藉由阻断细胞复制必须之叶酸依赖性代谢过程,达到抗肿瘤的功效。「培美曲塞」的结构、制备方法和抗癌活性等发明核心,于1994年取得美国5,344,932号专利(’932号专利),并已于2016年6月到期[1]。
但在前述'932号专利权期间届至后,长江后浪掀起的专利战争大戏才正要上演。Eli Lilly公司凭借其后续申请之美国第7,772,209号「抗叶酸组合的治疗方法专利」(’209号专利)[2],不论是无效挑战抑或侵权诉讼等大大小小的战役,无战不胜、无往不利,至少抵御了六至七家学名药厂的围攻和侵门踏户,成功保有Alimta®丰厚的美国市场。
姑不论专利无效挑战的火花四射,侵权诉讼的攻防广泛牵涉到「引诱侵权」和「均等侵权」等不同范畴的议题即精彩万分。例如「引诱侵权」的部分,本刊在第191期《学名药仿单是否构成方法专利引诱侵权?2017年Eli Lilly and Company v. Teva Parenteral Medicines案》一文中,曾介绍美国联邦巡回上诉法院(CAFC)在Teva案[3]指出:若药品仿单所建议的治疗(使用)方法尚受专利保护,制造并销售Alimta®学名药的药厂即可能构成引诱侵权[4]。本文在此则着重2019年Hospira案[5]和2020年Apotex案[6]等两件侵权诉讼中对’209号专利「均等范围解释」和以「申请历史禁反言」作为限制事项的攻防。
系争’209号专利
承前述,Alimta®活性药物成份的剂型为「培美曲塞二钠」(pemetrexed disodium),是一种抗癌效果良好的叶酸拮抗剂,但其不像标靶药物般具有对肿瘤细胞的特异性,所以不论是肿瘤细胞或是正常细胞内的叶酸均受其抑制,因此对施用的患者产生强烈的副作用。为减少「培美曲塞二钠」的毒性,’209号专利的权利范围包含在使用该药物前预先使用两种维他命:人工合成叶酸(folic acid)和维他命B12。以下说明本案主要攻防的请求项:
1. 一种对有需要的患者施用培美曲塞二钠的方法,包括:先施用一有效剂量的人工叶酸(folic acid)与一有效剂量的甲基丙二酸降低剂(methylmalonic acid),随后再施用一有效剂量的培美曲塞二钠,其中甲基丙二酸降低剂系选自,由维他命B12、羟基钴胺素(hydroxycobalamin)、cyano-10-chlorocobalamin、aquocobalamin perchlorate、aquo-10-cobalamin perchlorate、azidocobalamin、cobalamin、cyanocobalamin、或 chlorocobalamin所组成之群组。
12. 一种对化疗病人施用培美曲塞二钠之改良方法,其中改良处包括:
a) 在第一次施用培美曲塞二钠前施用介于约350 μg到约1000 μg的人工叶酸;
b) 在第一次施用培美曲塞二钠前施用介于约500 μg到约1500μg的维他命B12;且
c) 施用培美曲塞二钠。
多家学名药厂循505(b)(2)途径申请不同剂型的培美曲塞上市
承前所述,Alimta®为Eli Lilly公司最畅销的产品之一,众多学名药厂无不虎视眈眈,想方设法突破专利重围,争食这块市场大饼。这时’209号专利即展现一夫当关,万夫莫敌的气概。
除本刊曾介绍的Teva公司直接仿制Alimta®的活性药物成份「培美曲塞二钠」(pemetrexed disodium),在’932号结构专利权期间届至后申请学名药上市,但在专利侵权诉讼中被判「引诱他人侵害’209号治疗方法专利」外。本文则主要介绍其他多家学名药厂,包含Dr. Reddy公司、Hospira公司和Apotex公司,另以改良「培美曲塞」剂型的方式循505(b)(2)途径申请上市,以祈能够回避’209号专利的文义范围的图谋。
然而,无论是Dr. Reddy公司和Hospira公司研制的「培美曲塞双三羟甲基氨基甲烷」(pemetrexed ditromethamine),还是Apotex公司研制的「培美曲塞磷酸氢二钾」(pemetrexed dipotassium),均分别在2019年9月和2020年12月被CAFC维持联邦地院判决,判定落入’209号专利的均等范围。上述两个判决均对’209号专利的均等侵权与申请历史禁反言的攻防有详细的理由,为探讨治疗方法专利中药物剂型适用均等论的良好案例。
专利均等侵权与申请历史禁反言
在进入本案专利侵权诉讼的攻防战场前,首先说明专利侵权诉讼案件包括两种侵权类型:「文义侵权」及「均等侵权」。被控侵权对象未落入系争专利权之文义范围,应再分析其是否落入系争专利权的均等范围[7]。
所谓均等范围,是为防止当被控侵权对象在实施系争专利发明时,刻意选择请求项(申请专利范围)其中一个或多个组件,加以置换或修改,藉此区别与系争专利请求项的技术内容,以致不符合全要件原则下的文义侵害。此时,专利权人可援引均等论,主张被控对象与专利为实质相同而构成均等侵权[8]。然而,由于均等侵权的认定实质上扩大文义侵害的范围,为确保等侵权的正当性,法院在判断被控侵权对象是否构成均等侵权前,应先审查系争专利是否具有均等论之限制事项(limitation)[9]。
「申请历史禁反言」即为限制事项的攻防重点之一。若专利权人于专利申请过程或维护专利过程中所为之修正、更正或申复,若导致限缩申请专利范围,即不得再藉由均等论重新为主张其已放弃之专利权,以避免增加申请专利范围的不确定性[10]。本文以下继续说明与Eli Lilly公司Alimta®案相关的两项重要争点。
1. 重要争点一:’209号专利的均等范围扩张至所有「培美曲塞」剂型
美国最高法院在1997年于Warner Jenkinson案确立在专利侵权均等论的分析时,应采取「逐项测试法」(element-by-element test)。该测试法将被控侵权对象所实施的技术内容与专利权范围的技术特征逐一且个别比对,当两者有个别技术特征存在非实质差异(insubstantial difference)时,方成立均等构成侵害[11]。
CAFC在2019年Hospira案以「三部测试法」(tripartite test)检视’209号专利请求项12中对患者施用「培美曲塞二钠」的技术特征是否与被控侵权对象对患者施用的其他「培美曲塞剂型」时,存在非实质性差异[12]。亦即判断对患者施用「培美曲塞二钠」或其他「培美曲塞剂型」,是否构成以实质相同的方式(way),执行实质相同的功能(function),而得到实质相同的结果(result)。
首先,CAFC同意联邦地院将「施用培美曲塞二钠」(administration of pemetrexed disodium)解释为「将固态培美曲塞二钠溶于溶液中以施用液态培美曲塞二钠」的看法[13]。因此,被控侵权对象之一的Dr. Reddy公司主张,不论系争「培美曲塞」(pemetrexed)的抗癌针剂是由什么样的剂型组成,施打前均如联邦地院的解释,需先将其溶于注射剂溶液中,但’209号专利所保护施用「培美曲塞二钠」剂型中的钠盐(sodium)和其所使用「培美曲塞双三羟甲基氨基甲烷」(pemetrexed ditromethamine)剂型中的三羟甲基氨基甲烷(Tris),不论是缓冲能力、溶解度还是溶解到注射剂溶液后的pH值均在化学特性上有显著的不同。
然而,CAFC并不认同Dr. Reddy公司将判断焦点限缩在不同剂型的化学特性上,而是同意联邦地院的判断结果。联邦地院认为,Dr. Reddy公司的剂型会与专利权范围的「培美曲塞二钠」剂型均是以同样配制注射剂溶液的方式,产生相同数量的「培美曲塞」到患者罹患癌症的部位,而得到相同的治疗效果,故判断两者均等[14]。
于是,在法院「三部测试法」的判断结果下,’209号专利权范围从施用「培美曲塞二钠」实质均等扩张至施用所有「培美曲塞剂型」;亦即,不论对病患施用何种培美曲塞剂型,均受’209号专利权的保护。均等范围的扩张可参考下方示意图。
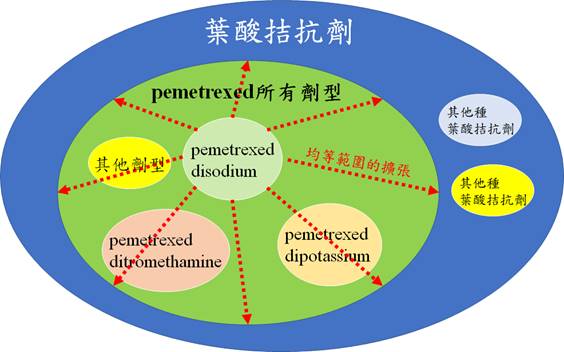
’209号专利权均等范围扩张示意图;制图:李秉燊
2. 重要争点二:’209号专利不受「申请历史禁反言」的限制
在阻止法院依均等论扩张’209号专利权利范围不成后,被控侵权人Dr. Reddy公司、Hospira公司和Apotex公司均在各自的诉讼中积极主张’209号专利应受「申请历史禁反言」的限制,进而直接阻却均等论的适用。
● 被控侵权人的重要主张包含:
(1) ’209号专利为美国第10/297,821号专利申请案(’821申请案)的延续案。’821申请案的申请过程中,原先是以「施用叶酸拮抗剂」(administration of antifolate)治疗哺乳动物为请求,但在审查过程中审查官检索到一篇科学期刊文章[15]已揭示「当对小白鼠施用叶酸拮抗剂前先喂食维他命B12时,可有效降低叶酸拮抗剂的毒性」。因此,申请人将「施用叶酸拮抗剂」(administration of antifolate)限缩至「施用培美曲塞二钠」(administration of pemetrexed disodium)时,已放弃施用培美曲塞二钠以外剂型的均等范围[16]。
(2) ’209号专利的申请过程中,除如前述将独立项的权利范围限缩至「施用培美曲塞二钠」,亦同时将「施用Alimta®」的附属项删除。由于通常知识之人均理解,Alimta®的活性药物成份为「培美曲塞」(pemetrexed),若将两者合并观察,应认为申请人已放弃施用培美曲塞二钠以外剂型的均等范围[17]。
● CAFC针对以上主张予以以下判定:
(1) CAFC认为,就‘821申请案将「施用叶酸拮抗剂」限缩至「施用培美曲塞二钠」等技术之修正理由,实与选择施用何种「培美曲塞剂型」毫无关联,故与诉讼中就该技术特征拟主张的均等范围「关连性甚低」(tangential relation),而不受申请历史禁反言的限制。
法院指出,’821申请案的限缩目的,只是为了回避科学期刊揭露「施用叶酸拮抗剂」的技术特征,且在限缩该等专利范围的同时,申请人在答辩过程中明确指出其如何发现施用「培美曲塞」是比单纯或随机施用「叶酸拮抗剂」更为有效,而未谈及任何有关培美曲塞「剂型」的问题;所以申请人并未放弃施用培美曲塞二钠以外剂型的均等范围[18]。
(2) CAFC认为,申请人将「施用Alimta®」的附属项删除的原因仅是因为审查官援引审查基准(MPEP) 第2173.05(u)条有关不得使用商标(trademark)或商品名称(trade name)作为权利范围以避免专利范围不明确的规定,实与申请人是否放弃施用培美曲塞二钠以外剂型的均等范围无关[19]。
CAFC基于上述理由,最终维持地院认为’209号专利不受「申请历史禁反言」的限制判决。
小结
改变药物剂型的设计常为学名药厂回避原开发药厂专利权文义范围的策略之一,若学名药厂只是刻意对请求项中的剂型稍加改变,加以置换或修改,以求回避文义侵害,仍要进一步以「三部测试法」分析是否构成实质相同的方式、功能和结果。但在学名药被要求「同成分、同质量、同药效」的情况下,「三部测试法」似确立了学名药难以挣脱均等侵权布下之天罗地网的事实,此从本文中法院的判断理由即可推知。
故本文建议新兴或中小型制药厂商若针对美国市场欲循505(b)(2)途径申请不同剂型的药品上市,应亟思如何应用新兴或特殊传递途径的制剂或缓释剂型,并产生对病人更好的疗效。虽然研发风险相对单纯仿制提高不少,但唯有如此才能掌握利基市场,推出贴近顾客需求又具备差异化的药品,方为「老药新用」的真谛。
备注:
- 「培美曲塞二钠」(pemetrexed disodium)结构的美国专利为U.S. 5,344,932,于1991年由美国普林斯顿大学申请,嗣于1994年获准,期间亦申请专利权期间延长获准,故该专利权期间直至2016年6月24日正式届至。
- US7,772,209,专利名称为Antifolate combination therapies(抗叶酸组合疗法),2010年获准,专利权期间预计直至2021年11月24日方届至。
-
Eli Lilly and Company v. Teva Parenteral Medicines, Inc., 845 F.3d1357 (Fed. Cir. 2017).
- 杨智杰,学名药仿单是否构成方法专利引诱侵权?2017年Eli Lilly and Company v. Teva Parenteral Medicines案,北美智权报第191期,2017 年8月09日,http://www.naipo.com/Portals/1/web_tw/Knowledge_Center/Infringement_Case/IPNC_170809_0503.htm
-
Eli Lilly & Co. v. Hospira, Inc., 933 F.3d 1320 (Fed. Cir. 2019), cert. denied, 207 L. Ed. 2d 1052 (June 15, 2020).
-
Eli Lilly & Co. v. Apotex, Inc., No. 2020-1328, 2020 U.S. App. LEXIS 39973 (Fed. Cir. Dec. 21, 2020)
- 专利侵权判断要点,经济部智慧财产局,2016年2月,页1。
- 同前注,页52。
- 近期专利均等侵权理论文献可参,张哲伦,申请历史档案禁反言之现代类型及其政策功能─绝对禁反言与弹性禁反言之辩证,月旦法学杂志,第304期,2020年9月,第36-57页;沈宗伦,专利权均等侵害与禁反言法则之例外,月旦法学教室,第210期,2020年4月,第31-34页。
- 前揭注3,页52。
-
Warner - Jenkinson Co. v. Hilton Davis Chem. Co., 520 U.S. 17, 21 (1997).
-
supra note 5, at 1335.
-
Id., at 1327.
-
Id., at 1335.
-
Arsenyan, F.G., Myasishcheva, N.V., Sof'ina, Z.P. et al. Influence of methylcobalamin on the antineoplastic activity of methotrexate. 12 Pharm Chem J 1299–1304 (1978). https://doi.org/10.1007/BF00779212
-
supra note 5, at 1335.
-
supra note 6, at *8.
-
supra note 5, at 1335.
-
supra note 6, at *8.
好消息~北美智权报有微信公众号了!
《北美智权报》内容涵盖世界各国的知识产权新闻、重要的侵权诉讼案例分析、法规解析,以及产业与技术新知等等。
立即关注北美智权微信公众号→ NAIP_IPServices
~欢迎读者分享与转发~ |
 |
|
【本文只反映专家作者意见,不代表本报立场。】
 |
|
| 作者: |
李秉燊 |
| 现任: |
北美智权报 专栏作家 |
| 学历: |
美国杜克大学法学院硕士班
台湾地区交通大学科技法律研究所博士候选人
美国杜克大学法学院访问学者
台湾地区交通大学科技法律研究所硕士生(径升博士班)
台湾地区阳明大学医事技术暨检验学系硕士 |
| 专业资格: |
2018年度台湾地区专利师考试及格
2014年度台湾地区医事检验师考试及格 |
|
|
|

